

LUMAKRAS 的疗效在一项单组、开放标签、多中心试验 (CodeBreaK 100 [NCT03600883]) 中得到证实。符合条件的患者需要患有局部晚期或转移性 KRAS G12C 突变 NSCLC,在接受免疫检查点抑制剂和/或铂类化疗后病情进展,东部肿瘤协作组体能状态 (ECOG PS) 为 0 或 1,并且至少有一个可测量病变(根据实体肿瘤疗效评估标准 (RECIST v1.1) 定义)。
所有患者都需要在中央实验室使用 QIAGEN therascreen® KRAS RGQ PCR 试剂盒在肿瘤组织样本中前瞻性地鉴定出 KRAS G12C 突变 NSCLC。在总共 126 名入组受试者中,有 2 名 (2%) 因基线时无放射学可测量病变而无法进行疗效分析评估。在 124 名肿瘤组织中确认有 KRAS G12C 突变的患者中,112 名患者的血浆样本使用 Guardant360® CDx 进行了回顾性检测。78/112 名患者 (70%) 在血浆标本中发现 KRAS G12C 突变,31/112 名患者 (28%) 在血浆标本中未发现 KRAS G12C 突变,3/112 名患者 (2%) 因 Guardant360® CDx 检测失败而无法评估。
总共 124 名患者在基线时至少有一个可测量病变,由盲法独立中央审查 (BICR) 根据 RECIST v1.1 评估,并接受 LUMAKRAS 960 mg每日一次治疗,直至病情进展或出现不可接受的毒性。主要疗效结果指标是客观缓解率 (ORR) 和缓解持续时间 (DOR),由 BICR 根据 RECIST v1.1 进行评估。
研究人群的基线人口统计学和疾病特征为:中位年龄 64 岁(范围:37 至 80 岁),其中 48% ≥ 65 岁,8% ≥ 75 岁;50% 女性;82% 白种人,15% 亚裔,2% 黑人;70% ECOG PS 1;96% 患有 IV 期疾病;99% 为非鳞状组织学;81% 为前吸烟者,12% 为当前吸烟者,5% 为从不吸烟者。所有患者均接受过至少 1 种转移性 NSCLC 全身治疗;43% 仅接受过 1 种治疗,35% 接受过 2 种治疗,23% 接受过 3 种治疗; 91% 接受过抗 PD-1/PD-L1 免疫治疗,90% 接受过铂类化疗,81% 同时接受过铂类化疗和抗 PD-1/PD-L1 治疗。已知的胸外转移部位包括 48% 的骨、21% 的脑和 21% 的肝脏。
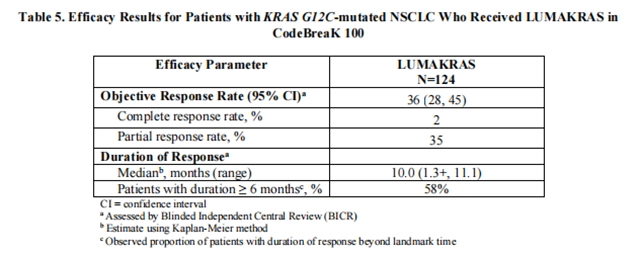
疗效结果总结于表 5。
FDA,2023.04
索托拉西布是一种针对携带 KRAS 基因 p.G12C 突变的晚期非小细胞肺癌(NSCLC)患者的靶向治···【more】
推荐阅读:280发布时间:2024-09-07
在一项 1 期研究中 ,Sotorasib索托拉西布对KRAS p.G12C 突变的晚期实体瘤患者显示出抗癌活性,并且在非小细胞肺癌 (NSCLC)患者亚组中观察到特别有前景的抗癌活性。在一项单组 2···【更多】
文章来源:卢修斯制药发布时间:2024-11-15推荐人数:249

卢修斯制药有限公司公司2020年成立于老挝首都万象。其宗旨是为全球提供安全、有效且实惠的药品。公司工厂占地210000平方米,生产覆盖多个治疗领域的200多种仿制药,涵盖多个治疗领域,为患者提供了高质量且经济可负担的治疗选择。
地址:No.26 Thongmang village, Xaythany district, Vientiane Capital
邮箱:info@lucius.la
电话:+856 309560384
电话:+856 2052137046

微信